Class 12th Chemistry Chapter 3 रासायनिक बलगतिकी part 4 रासायनिक बलगतिकी का ही एक अहम् भाग है | अगर आप इस इकाई अथवा पाठ को अच्छे से अध्ययन करना चाहते है तो हम आपसे यही अनुरोध करते है कि आप इस बहुत बड़ी इकाई को छोटे छोटे part में पढ़े | यही वजह है कि हम आपको यहाँ पर part वाइज नोट्स Provide कर रहे है | इस part में जो भी महत्वपूर्ण हैडिंग है उन्हें जरूर याद करे | क्यूंकि ये ही आपको अच्छे मार्क्स प्राप्त करने में मदद करेंगी |
Table of Contents
ToggleIf you need online tutor or help for any questions like mathematics, physics, chemistry numerical or theory then you can contact me on WhatsApp on +918755084148 or click here. Our team help you all time with cheap and best price. If need it on video our team provide you short video for your problem. So keep in touch of our team specialists.
Class 12th Chemistry Chapter 3 रासायनिक बलगतिकी part 4
इस भाग में हम बोर्ड में पूछे गये कम से कम 3 से 5 मार्क्स का अध्ययन करेंगे | अत: आप इन्हें ध्यान से पढ़े | अगर आप कुछ समस्या महसूस करते है तो आप हमे सम्पर्क कर सकते हो और आप Ask Question पर क्लिक करके प्रश्न भी पूछ सतके हो | हम आपसे ये गुजारिश करते है कि आप इन महत्वपूर्ण हैडिंग को अवस्य याद करेंगे | क्यूंकि ये वो सभी हैडिंग है जो पिछले बहुत सालो के पेपर में रिपीट हुई है | अगर आप इन्हें याद करके एग्जाम में बैठते है तो आप 90 % से अधिक अंक हासिल कर सकते है |
Class 12th Chemistry Chapter 3 रासायनिक बलगतिकी part 4 में महत्वपूर्ण Headings निम्नलिखित है | इन्हें अच्छे से याद करे | ये आपको अच्छे अंक दिलाने में मदद करेगी:
- द्वितीय कोटि की अभिक्रिया और इसके अभिलक्षण
- तृतीया कोटि की अभिक्रिया और इसके अभिलक्षण
- आभासी आणविक अभिक्रियाए और अभिक्रिया की कोटि का निर्धारण
- संघट्ट वाद सिद्धांत और सक्रियण उर्जा
- प्रभावी टकरे सक्रिय अणु और देहली उर्जा
- सक्रियण उर्जा का महत्व और आर्हिनियस समीकरण

क्या जरूर्री है क्या नही :-अच्छे से अच्छे अंक लाने के लिए आपको बेहतर नोट्स एंड बेहतर क्लास लेनी चाहिये जो आपको बिलकुल फ्री में हम यहाँ पर दे रहे है |
अत: अच्छे से हमारी वेबसाइट https://excellentshiksha.com/ से पढे हम आशा करते है की आप बेहतर अंक प्राप्त करेंगे |
द्वितीय कोटि की अभिक्रिया और इसके अभिलक्षण
द्वितीय कोटि की अभिक्रिया :- वे अभिक्रिया जिनका वेग अभिकारक की सांद्रता के द्वितीय घात के अनुक्र्मानुपति होता है, द्वितीय कोटि की अभिक्रिया कहलाती है|
जैसे :- एस्टर का क्षार के द्वारा अपघटन ;-
CH3COOC2H%+ NaOH ————-> CH3COONa + C2H5OH
ओजोन का ऑक्सीकरण :- ओजोन का ऑक्सीकरण विद्युत विसर्जन द्वारा किया जाता है
2O3 ———————> 3O2
द्वितीय कोटि की अभिक्रिया के अभिलक्षण :- इसके निम्नलिखित लक्ष्ण है –
1- इस प्रकार की अभिक्रिया का अर्धायुकाल अभिकारक की प्रारम्भिक सांद्रता पर निर्भर करता है| इसे निम्न सूत्र द्वारा ज्ञात किया जाता है –
t1/2 = 1/ k [R0]
2- इस प्रकार की अभिक्रिया का वेग स्थिरांक अभिकारक की सांद्रता पर निर्भर करता है| अर्थात आप सांद्रता में परिवर्तन करते है , तो वेग स्थिरांक भी परिवर्तित हो जाता है|
3- इस अभिक्रिया में वेग स्थिरांक का मात्रक लीटर प्रति मोल प्रति सेकंड होता है|
तृतीया कोटि की अभिक्रिया और इसके अभिलक्षण
तृतीया कोटि की अभिक्रिया :- वे अभिक्रिया जिनका वेग अभिकारक पदार्थ की सांद्रता की तृतीया घात पर निर्भर करता है तृतीय कोटि की अभिक्रिया कहलाती है |
जैसे :-
2FeC3 + SnCl2 ——————-> 2FeCl2 + SnCl4
2NO + O2 ————-> 2NO2 आदि
तृतीय कोटि की अभिक्रिया के लक्ष्ण :- इस अभिक्रिया के निम्नलिखित लक्ष्ण है –
1- इस अभिक्रिया का अर्धायुकाल अभिकारक की सांद्रता के वर्ग के व्युत्क्रमानुपाती होता है|
2- इस अभिक्रिया के वेग स्थिरांक का मात्रक वर्ग लीटर प्रति वर्ग मोल प्रति सेकंड होता है|
आभासी आणविक अभिक्रियाए और अभिक्रिया की कोटि का निर्धारण
आभासी आणविक अभिक्रियाए :- एसी रासायनिक अभिक्रियाए जिनकी कोटि और आण्विकता का मान समान नही होता है , आभासी आणविक अभिक्रिया कहलाती है |इन्हें छदम कोटि की अभिक्रिया भी कहा जाता है |
अर्थात
” एसी अभिक्रिया जिनकी कोटि एक परन्तु आण्विकता दो या दो से अधिक होती है | आभासी अथवा छदम एकानुक अभिक्रिया कहलाती है|
जैसे :-
CH3COOC2H5 + H2O ——————–> CH3COOH + C2H5OH
अभिक्रिया की कोटि का निर्धारण :- अभिक्रिया की कोटि को विधियों द्वारा निर्धारित किया जा सकता है :-
1- समाकलन विधि द्वारा 2- अर्धायुकल विधि द्वारा 3- ओस्टवाल्ड प्रथक्करण विधि द्वारा 4- ग्राफीय विधि द्वारा
इनके बारे में हम अगली कक्षों में पढ़ेंग |
संघट्ट वाद सिद्धांत और सक्रियण उर्जा
संघट्ट वाद सिद्धांत :- यह सिद्धांत यह मानकर चलता है की केवल उन अणुओ के टकराने से अभिक्रिया होती है जिनके पास अपनी सामान्य औसत उर्जा के सापेक्ष अतिरिक्त न्यूनतम उर्जा होती है |जो अभिकारको की सक्रियण उर्जा कहलाती है |
इस सिद्धांत के अनुसार अभिक्रिया का ताप बढ़ाकर वेग बढ़ाया जा सकता है ,लेकिन एसा सभी अभिक्रियाओ में नही होता है|
इसे निम्न सूत्र द्वारा ज्ञात किया जा सकता है –
प्रभावी टकरे सक्रिय अणु और देहली उर्जा
यह सिद्धांत निम्न लिखित अवधारणाओ पर आधारित है –
1- रासायनिक अभिक्रिया होने के लिए कम से कम दो अणुओ का टकराना आवश्यक होता है|
2- अभिकारको के परमाणुओ के टकराने से उनके मध्य अभिक्रिया नही होती है| जबकि अभिक्रिया जिन टकरो के फलस्वरूप होती है , उन्हें प्रभावी टकरे कहते है| इनकी संख्या बहुत कम होती है |
3- प्रभावी टक्कर में भाग लेने वाले अणु को सक्रिय अणु कहा जाता है इन अणुओ की उर्जा एक निश्चित उर्जा तल के बराबर या इससे अधिक होती है, इस उर्जा तल को देहली उर्जा कहते है |
4- अभिकारक के अणु में निहित प्रारम्भिक उर्जा तल को सक्रिय करके देहली उर्जा तक ले जाने हेतु अवश्यक अतिरिक्त उर्जा की मात्रा को उस अणु की या अभिक्रिया की सक्रियण उर्जा कहते है |
सक्रियण उर्जा = देहली उर्जा – अनुओ की टक्कर से पूर्व निहित उर्जा
5- इस सिधांत के अनुसार अभिक्रिया का वेग उस अभिक्रिया में भाग लेने वाले अणुओ की प्रभावी टक्कर की संख्या पर निर्भर करता है|
6- सक्रियण उर्जा को जुलो प्रति मोल अथवा कैलोरी प्रति मोल में नापते है|
सक्रियण उर्जा का महत्व और आर्हिनियस समीकरण
सक्रियण उर्जा का महत्व :- इससे हमे निम्न जानकारी प्राप्त होती है –
1- अभिक्रिया वेग के बारे में पता लगाया जा सकता है| यदि सक्रियण उर्जा अधिक है तो अभिक्रिया का वेग अधिक होता है अन्यथा नही |
2- अभिक्रिया के ऊष्माक्षेपी और ऊष्मा शोषी का भी पता लगाया जा सकता है|
3- यदि किसी अभिक्रिया की सक्रियण उर्जा शून्य है तो उस पर तापमान का कोई भी प्रभाव नही पड़ता है|
4- सामन्यत: ताप मान में 10 डिग्री सेल्सियस बढ़ाने से अभिक्रिया का वेग दो गुना हो जाता है|
आर्हिनियस समीकरण :- वैज्ञानिक आर्हिनियस ने अभिक्रिया के वेग पर ताप के प्रभाव को समझने के लिए एक समीकरण प्रस्तुत की जो आर्हिनियस समीकरण के नाम से जनि गयी –
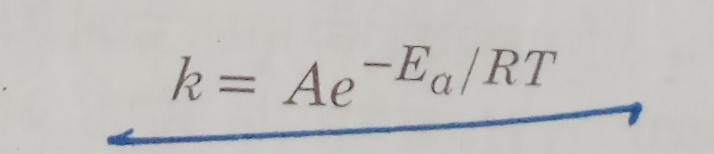
जहाँ A को पूर्व चरघातांकी गुणांक या अवर्त्ति गुणांक भी कहते है और Ea सक्रियण उर्जा , R गैस स्थिरांक तथा T ताप मान और k वेग स्थिरांक है |
………….THE END ……………














